Se conoce como materia a todo aquello que posee una masa, que ocupa un lugar en el espacio y que se convierte en energía. Cuando se habla de propiedades de la materia se refieren a aquellas características químicas y físicas que la componen y describen. Además la materia también tiene distintos estados.
A continuación conoceremos en detalle cada uno de ellos.
| Materia | |
| Definición | Todo aquello que ocupa un lugar observable en el espacio y que tiene determinada cantidad de energía asociada. |
| Propiedades |
-Propiedades generales o extrínsecas: son las características que comparte toda la materia, sin diferencias en forma, composición, elementos que la componen o presentación. -Propiedades específicas o intrínsecas: son las características que diferencian a las sustancias. |
| Estados | Son las distintas fases de agregación que los que puede encontrarse la misma, ya seas sustancias puras o mezclas. Los estados de la materia pueden ser: solido, liquido, gaseoso y plasmático |
¿Qué es la materia?
La materia es todo aquello que ocupa un lugar observable en el espacio y que tiene determinada cantidad de energía asociada. Es aquello de los que esta hecho el universo y que además, se puede medir de alguna manera.
Se puede definir a la materia como todo lo que posee masa, ocupa un lugar, dura en el tiempo y que además puede ser medible con algún instrumento de medición especifico.
La materia tiene propiedades y tiene estados. Con respecto a las propiedades de la misma, se pueden dividir en propiedades generales que son las que tienen en común todos los cuerpos y no permiten diferencias una sustancia de otra, y las propiedades especificas que son aquellas intrínsecas de la materia que si permiten diferenciar a un cuerpo de otro.
Con respecto a los estados de la materia, son las distintas fases de agregación que los que puede encontrarse la misma, ya seas sustancias puras o mezclas. Los estados de la materia pueden ser: solido, liquido, gaseoso y plasmático.

Propiedades de la materia
Las propiedades de la materia pueden diferenciarse en generales o especificas. Cuando nos referimos a las propiedades generales estamos hablando a las cualidades físicas que tiene la misma.
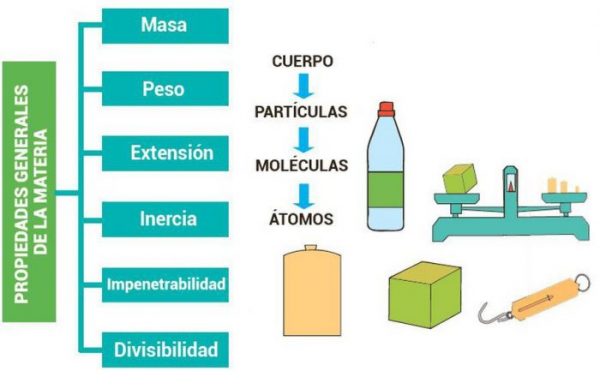
–Propiedades generales o extrínsecas: son las características que comparte toda la materia, sin diferencias en forma, composición, elementos que la componen o presentación. Estas propiedades no permiten diferenciar una sustancia de la otra. Dentro de estas propiedades podemos encontrar:
- Extensión: es el espacio o volumen que ocupa dentro de un determinado cuerpo.
- Masa: es la cantidad de materia que posee un cuerpo.
- Inercia: es la capacidad que tiene de conservar su estado de reposo o movimiento sin intervención de una fuerza.
- Porosidad: es el espacio que existe entre las partículas de un cuerpo.
- Divisibilidad: refiere a la capacidad de subdivisión en partes más pequeñas que tiene la materia.
- Peso: es la fuerza que ejerce la gravedad sobre un cuerpo material.
–Propiedades específicas o intrínsecas: son las características que diferencian a las sustancias. Las mismas pueden ser propiedades físicas, es decir aquellas que posee la materia sin que cambie su naturaleza, y propiedades químicas que son las características en las que si hay un cambio en la composición de la materia, como por ejemplo puede ser la oxidación.
- Propiedades físicas: las mismas definen la forma y el estado en la que podemos medir a la materia. Las mismas son:
-Densidad: es la cantidad de masa por unidad de volumen. Cada material posee su propia densidad.
-Punto de fusión: es la temperatura a la que la sustancia cambia del estado sólido al estado líquido.
-Conductividad eléctrica: es la capacidad que tiene un material para conducir la corriente eléctrica por medio de su estructura. Hay ciertos materiales que son buenos conductores como los metales, y otros que son aislantes, tales como el plástico, el vidrio y la madera.
-Conductividad térmica: es el grado o la medida en que un material puede conducir calor.
-Punto de ebullición: es la temperatura a la cual la presión de vapor de un líquido se equipara a la presión que rodea al líquido provocando que el líquido se transforme en gas.
- Propiedades químicas: estas propiedades son las que definen la reactividad de la materia, es decir cuando una materia se convierte en otra por medio de una reacción química. Las propiedades químicas son:
-Reactividad: es la capacidad que posee una sustancia para reaccionar en presencia de otra sustancia.
-Combustibilidad: es la capacidad de una sustancia para combustionar. Es decir provocar una reacción de oxidación, generando incluso hasta explosiones.
-Acidez: es la característica que posee una sustancia de comportarse como un ácido.
–Alcalinidad: es la capacidad que posee una sustancia para contrarrestar el efecto de un ácido, esto quiere decir para neutralizarlo.
Estados de la materia
Se conoce como estados de la materia a las diferentes fases de agregación en las que puede encontrarse una materia. Este estado de agregación va a depender del tipo y de la intensidad de las fuerzas de unión que existan entre sus partículas. Además otros de los factores que influyen en los estados de la materia son la temperatura y la presión.
Los estados de la materia son: solido, liquido, gaseoso y de manera menos frecuente el estado plasmático. Cada uno de estos estados tiene características o propiedades físicas distintas.
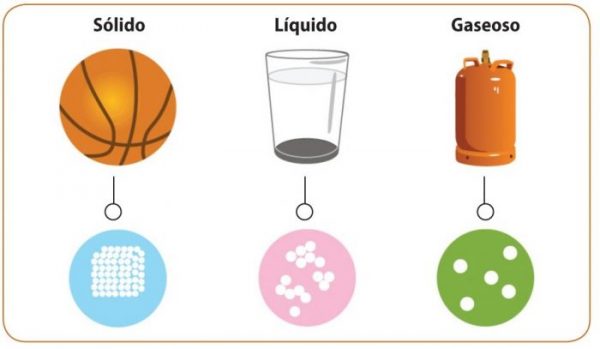
Estado solido
Es el estado de la materia donde sus partículas están muy juntas y unidas por una fuerza de atracción de una gran magnitud. Es por esta razón que los solidos poseen una forma bien definida, de gran densidad y resistencia a la fragmentación.
Los solidos tienen una baja o casi nula fluidez, y al fragmentarlos se obtienen solidos más pequeños. Ejemplos de sólidos: los minerales, los metales, la piedra, los huesos, la madera.
Estado líquido
El estado liquido se caracteriza por tener partículas que están unidad por una fuerza de atracción pero más débil que la de los solidos. Es por esta razón que los líquidos no tienen una forma definida y estable ni tampoco tienen resistencia. Poseen una gran fluidez, de hecho adquieren la forma del envase que los contenga. Ejemplos de líquidos: el agua, el mercurio, la sangre.
Estado gaseoso
El estado gaseoso es aquel en el cual las partículas se encuentran en un estado de dispersión y alejamiento de tal manera que apenas pueden mantenerse juntas. La fuerza de atracción de las mismas es muy débil y están en un estado desordenado. Ocupan un volumen mayor que los solidos y los líquidos, ya que un gas tiende a expandirse hasta ocupar la totalidad del espacio en el que se encuentre. Ejemplos de gases: el aire, el dióxido de carbono, el nitrógeno, el helio.

Estado plasmático
Este estado es poco común, y es aquel en el que la materia puede comprenderse como un gas ionizado, esto significa que esta compuesto por átomos a los que se les ha sumado o restado electrones. El plasma es un gran transmisor de electricidad.
El plasma tiene características propias, que no concuerdan con las de los demás estados de la materia, es por eso que se lo denomina como un cuarto estado.
El plasma puede ser frio o caliente. El frio es aquel en el cual la temperatura de los electrones es mayor a la de las partículas pesadas. Por otro lado el plasma caliente es aquel en el cual los átomos ionizados adquieren una gran temperatura cuando chocan de manera continua y esto genera luz y calor. Ejemplos de plasma: el sol, las pantallas electrónicas, el interior de los tubos fluorescentes.