En química se llaman ácidos y bases a dos tipos diferentes de sustancias opuestas entre sí, cada una de éstas sustancias reúne propiedades específicas que modifican el comportamiento de las soluciones químicas. Tanto ácidos como bases pueden encontrarse en estado líquido, gaseoso y sólido.
Al juntarse ácidos y bases en unaa solución se produce una reacción exotérmica, es decir, se produce calor, esta reacción se conoce como neutralización.
| Clasificación de Ácidos y Bases | Características | Ejemplo |
| Ácido Fuerte | Es un ácido que se ioniza completamente en solución acuosa | HCI (ac) H2SO4(ac) |
| Base Fuerte | Es una base que se ioniza completaamente en solución acuosa | NaOH (ac) KOH (ac) |
| Ácido Débil | Es un ácido que se ioniza parcialmente en solución acuosa, por lo que la concentración de sus iones en solución es menor que la de un ácido fuerte | Ácido Carbónico (H2 CO3) |
| Base Débil | Es una base que se ioniza parcialmente en solución acuosa, por lo que la concentración de sus iones en solución es menor que laa de una base fuerte | Amoníaco (NH3) |
¿Que es un Ácido?
Se llaman ácido a aquellas sustancias que liberan iones de hidrógeno positivos (H+) en una solución. Los ácidos tiene un sabor agrio y hscen que ciertos colorantes se tornen rojos. Algunos ácidos elaborados por el cuerpo, como el ácido gástrico pueden ayudar aa los órganos aa funcionr correctamente.
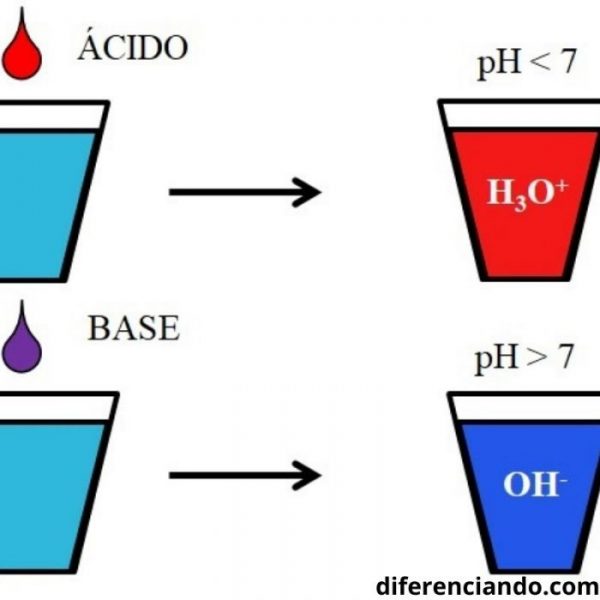
Propiedades de los ácidos
- Tienen sabor aamargo como el ácido de los cítricos.
- Son corrosivos.
- Cambia el color del papel de aazul a rosa y de anaranjado a rojo.
- Producen quemaduras en laa piel.
- Son buenos conductores de la electricidad en soluciones acuosas.
- Reaccionan con metales activos formando sal e hidrógeno.
- Reaccionan con bases formando sal más agua.
- Reaccionan con óxidos metálicos para formar sal más agua.
Ejemplos de Ácidos
- Ácido Perclórico: es un ácido fuerte líquido a temperatura ambiente, altamente oxidante.
- Ácido Nítrico: es un ácido fuerte e intensamente oxidante, empleado para fabricar ciertos explosivos y también fertilizantes.
- Ácido Ascórbico: es la vitamina C, tan necesaria para la salud, es una sustancia protectora por sus efectos antioxidantes.
- Ácido Clorhídrico: Es el único ácido fuerte que sintetiza el cuerpo humano, proceso que ocurre en el estómago para llevar a cabo laa degradación de los alimentos en el proceso digestivo.
- Ácido Tartárico: es un polvo cristalino blanco, se utiliza en la preparación de bebidas efervescentes, en la industria panadera, vitivinícola y farmacéutica. El cremor tártaro que llevan algunas recetas es ácido tartárico.
- Ácido Fluorhídrico: por su capacidad de atacar al vidrio, se lo usa en el tallado y grabado de cristales.
- Ácido Sulfúrico: es un ácido fuerte por excelencia tiene infinidad de aplicaciones en diversas industrias y proceso de síntesis.
- Ácido Trifluoroacético: es un buen disolvente para muchos compuestos orgánicos.
- Ácido Fosfórico: está presente en variaas bebidas colas. Se consideraa perjudicial para la salud, ya que promueve la descalsificación.
- Ácido acético: es el principal componente del vinagre, la cidez que crea lo transforma en un conservante de alimentos muy utilizado.
- Ácido Fluorontimónico: es el superácido más fuerte que se conoce, supera la acidez del ácido sulfúrico.
- Ácido Crómico: es un polvo rojo oscuro, participa del proceso del cromado, además se lo utiliza paara esmaltar cerámicas.
- Ácido Indolacético: es el principal representante de las auxinas, importnte en hormonas de crecimiento de las plantas.
- Ácido desoxirribonucleico: es el que encierra la clave de la vida ya que conforma los genes que gobiernan la síntesis de infinidad de proteínas.
- Ácidos Tricarboxílicos: comprende un grupo de ácidos carboxílicos que tienen tres grupos carbóxilos
- Ácido Fórmico: es el más sencillo de los ácidos orgánicos, la exposición prolongada a éste ácido puede causar fallo respirtorio y la muerte.
- Ácido Glucónico: las sales de este ácido son muy empleadas en procesos de limpieza de objetos de vidrio.
- Ácido Láctico: forma parte importante de procesos bioquímicos.
- Ácido Benzoico: es un ácido con un olor característico que se utiliza mucho para conservar alimentos que requieren un PH ácido.
- Ácido Málico: es muy utilizado en la industria farmacéutica para laa fabricaación de laxantes.
- Ácido caarbónico: en algunos lugares forma parte del proceso de formación de las cuevas. Esta presente en bebidas gaseosas.
- Ácido Acético: es el ácido débil que usamos en la ensalada
- Ácido Acetilsalicílico: es el principio activo de la aspirina, medicamento que se utiliza como analgésico.
- Ácido Ascórbico: es el nombre común de la vitamina C, que se encuentr en frutas y suplementos vitamínicos y que participa de la cicatrización.
- Ácido Bórico: es un ácido débil que se usa como insecticida y retardante de llama.
- Ácido Butírico: es el ácido graso presente en la manteca.
- Ácido Carbónico: es el áacido que se encuentra en las bebidas gaseosas.
- Ácido Fólico: es un ácido que se consigue en las hojas de los vegetales.
- Ácido Hialurónico: se usa en cremas para la piel.
- Ácido Oléico: ´cido graaso que se encuentra en el aceite de oliva.
- Ácido Oxálico: ácido que se consigue en las hojas de espinaca.
- Ácido Úrico: su exceso en laa sangre se conoce como hiperuricemia.
- Ácido Araquidónico: ácido graso que se encuentra en las membranas celulares.
- Ácido Retinoico: es un áacido producto del metabolismo de la vitaamina.
- Ácido Linoleico: ácido que se encuentr en las nueces.
Ejemplos de Bases
- Hidróxido de Sodio: es una base fuerte que se utiliza en la industria papelera.
- Hidróxido de Magnesio: es unaa base fuerte que a veces se utiliza como ntiácido o laxante.
- Hidrógeno de Calcio: se emplea para fabricar pesticidas.
- Hidrógeno de Potasio: es una base fuerte y corrosiva que se emplea mucho en diferentes industrias, muy utilizado para faabricar jabón.
- Hidrógeno de Bario: se utiliza para fabricar vevenos.
- Hidrógeno de Hierro II o III: suele generarse con la industria metalúrgica, se utiliza para fabricar pintura.
- Amoníaco: es un gas con un olor característico, se utiliza para fabricr fertilizantes.
- Jabón: es una sal de sodio o potasio, se utiliza para higiene personal.
- Detergente: también es un producto para laa higiene.
- Quinina: es una base natural producida por algunas plantas, tiene propiedades analgésicas.
- Anilina: se emplea en la industria del caucho, en la fabricación de esplosivos entre otras cosas.
- Guanina: es una de las bases nitrogenadas que forma parte de los ácidos nucleicos.
- Pirimidina: las bases nitrogenadas que conformn los ácidos nucleicos son derivdos de la pirimidina.
- Citosina: es una de las bases nitrogenadas que forman parte de los ácidos nucleicos.
- Adenina: es también una de las bases que forman parte de las ácidos nucleicos.
- Hidróxido de Zinc: es una sustancia que puede actuar como ácido y como base a la vez.
- Hidróxido de cobre: se utiliza para dar color a objetos de cerámica.
- Hidróxido de Circonio: se utiliza en el vidrio
- Hidróxido de Berilio: es un sustancia de abundancia limitada.
- Hidróxido de Aluminio: se utiliza en l medicina como amtácido.
- Omeprasol: inhibe hsta el 80% la secreción de ácido clorhídrico.
- Lansoprazol: se utiliza pra tratar lesiones
- Esomeprazol: se utiliza paar disminuir la producción de ácido.
- Pantoprazol: Inhibidor de la bomba de protones.
- Rabeprazol: se utiliza en traatamientos a corto plazo.
Las carcterísticas de las bases se pueden mencionar que según la temperatura éstas pueden encontrarse en sustancias líquidas, sólidas o gaseosas, se pueden clasificar en bases fuerte y débiles, tiene un sabor amargo, varían según su grado de PH, en soluciones acuosas pueden ser conductores de electricidad y son corrosivas en diversos metales.